Em sessão plenária da semana passada expôs uma realidade que há tempos incomoda quem acompanha de perto as políticas de saúde pública: a lentidão do governo federal em regulamentar o uso da cannabis medicinal pelo SUS. O prazo, que já era apertado, foi novamente prorrogado por mais 180 dias, e, enquanto isso, milhares de pacientes continuam reféns de altos custos e da incerteza.
Deputados aliados do governo criticam
O deputado Padre Pedro Baldissera (PT) foi direto ao ponto: “a morosidade não é boa para os pacientes”. Tem razão. Em muitos casos, a cannabis não é luxo nem modismo, é alívio e qualidade de vida. Santa Catarina já deu o exemplo, regulamentando o uso medicinal em nível estadual, mas o que se espera é que o país todo siga o mesmo caminho, com segurança e empatia.

Já o deputado Marquito (Psol) também tocou num ponto essencial: as associações que hoje ajudam pacientes não podem ser esquecidas ou empurradas para a ilegalidade. Elas preenchem, com solidariedade, o vazio deixado pela falta de regulamentação federal.
Outubro Rosa
Entre críticas e elogios, a sessão também celebrou boas notícias: o Outubro Rosa e a ampliação da faixa etária para exames preventivos de câncer de mama, uma medida que salva vidas e precisa ser celebrada. Mas fica o contraste: enquanto uma política avança com sensibilidade e foco na prevenção, outra emperra em burocracia. E, nesse atraso, quem mais sofre é quem já carrega o peso da dor e da espera.





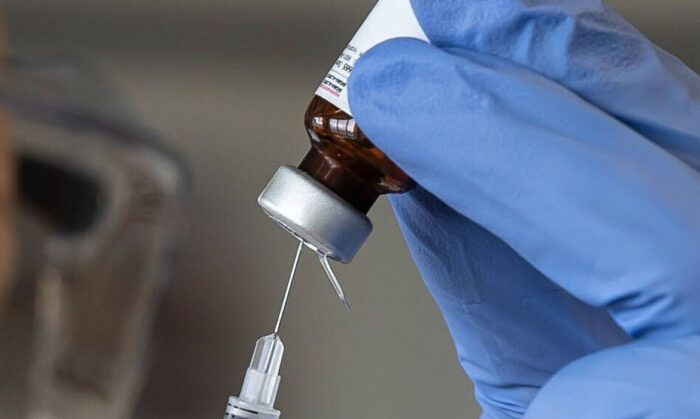
 A Anvisa (Agência Nacional de Vigilância Sanitária) decidiu nesta quinta-feira conceder autorização temporária de uso emergencial, em caráter experimental, de vacinas contra a Covid-19 e estabeleceu regras para que empresas solicitem a autorização.
A Anvisa (Agência Nacional de Vigilância Sanitária) decidiu nesta quinta-feira conceder autorização temporária de uso emergencial, em caráter experimental, de vacinas contra a Covid-19 e estabeleceu regras para que empresas solicitem a autorização. 